前沿生物:携抗艾药闯关科创板 能否扭亏为盈成疑|健康IPO
前沿生物于12月2日更新了2019年三季报财务数据,并再次发布问询回复意见,公司重新进入科创板发行上市审核流程。
投中健康12月9日讯,由于发行上市申请文件中记载的财务资料过有效期,而被上交所中止了上市审核的前沿生物于12月2日更新了2019年三季报财务数据,并再次发布问询回复意见,公司重新进入科创板发行上市审核流程。
根据招股说明书,前沿生物是一家创新型生物医药企业。其拥有一个国内上市的原创抗艾滋病创新药艾可宁,拥有两个处于美国II期临床阶段的在研新药,分别为艾可宁+3BNC117联合疗法,以及新型透皮镇痛贴片AB001。

根据招股说明书,前沿生物尚未实现盈利,报告期内,前沿生物累计亏损达到3.78亿元。亏损不断的原因,第一是因为前沿生物单一产品依赖严重,第二是因为目前在研产品还处在临床阶段,但研发需要较大的资金投入,这也是前沿生物谋求上市的原因,以覆盖研发费用。
作为唯一一款上市新药,艾可宁构成前沿生物营收主要来源。招股说明书显示,艾可宁是全球首例获批的长效HIV融合抑制剂,对主要流行 HIV-1 病毒、包括耐药病毒均有效。艾可宁于2018年5月取得国家药监局上市批件,自2018年8月起在国内销售。
在单一产品依赖严重的情况下,前沿生物前期研发投入资本化比例高。最新回复意见显示,前沿生物在2018年5月取得艾可宁新药上市批件后,便将相关研发支出转入无形资产核算,并按10年期限摊销。自开始III期临床研究至取得新药证书,艾可宁在开发阶段研发支出为1.85亿元,该部分支出全部资本化。按10年期限摊销,每年摊销成本为1851.83万元,但目前艾克宁2019年1—9月销售收入为1097.74万元,能否覆盖摊销成本具有较大的疑问。
疑问在于,目前艾可宁产能利用率、产销率都不太理想。根据前沿生物对上交所问询的最新回复,前沿生物艾可宁制剂产能为18万支。2018年、2019年1—9月,艾可宁的产能利用率分别为19.58%和22.33%;艾可宁产销率(已销售出去的产品与已生产的产品数量的比值)分别为14.02%和45.80%。
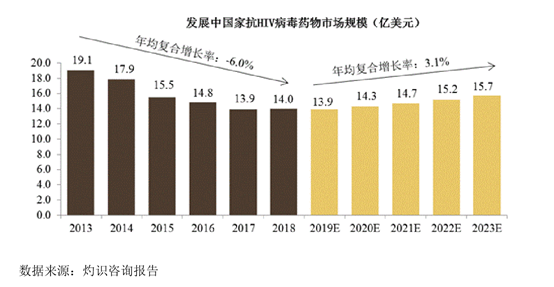
对此,前沿生物表示,虽然公司已开始艾可宁的商业化进程,但国内医生、患者对艾可宁的认知度仍需培育,国外市场开拓也需要一定时间,因此艾可宁的销售规模较小,如果艾可宁商业化进展较慢,则可能难以实现收入大幅度增长并实现盈利。根据灼识咨询的报告,目前发展中国家抗HIV病毒药物市场规模逐年下降,以UNAIDS 为主的一系列机构和组织以援助为目的降低销往该地区的抗HIV药物价格。而国内抗HIV病毒药物又主要以国家免费药物为主,前沿生物艾克宁未来收入压力较大。
在唯一上市产品产能利用率、产销率不足,对盈利构成巨大挑战的情况下,前沿生物寄希望于通过其他在研产品摆脱亏损状态。前沿生物在研发投入力度较大,报告期内,研发投入分别为 5476.23 万元、8355.43 万元、9943.77万元及 2012.23万元。但值得注意的是,前沿生物目前主要在研的两个项目中,艾可宁+3BNC117联合疗法、新型透皮镇痛贴片AB001来自专利授权或专利转让,这两款药存在专利到期风险、专利授权风险。
此外,前沿生物核心技术产品“艾博卫泰”(商品名为艾可宁)的共同发明人HE JIANG(姜和)早已离职。根据公开信息,“艾博卫泰”涉及三项核心发明专利,而这三项核心发明专利的发明人为DONG XIE(谢东)、HE JIANG(姜和),前沿生物因此收到上交所对其持续的新药研发能力的问询。前沿生物回应称,“公司通过外部收购或授权方式,规避了药物早期基础研究及候选药物阶段的不确定性”。
产能利用率不足、产销不饱、研发持续能力被怀疑,前沿生物能否借主营及研发产品扭亏为盈需要打一个大大的问号,其科创版IPO之路前景坎坷。
全部评论